Une intelligence artificielle retrouve des lois physiques à partir de données scientifiques
L'apprentissage profond est-il inévitablement synonyme de "boîtes noires"? On reproche souvent à ces méthodes leur absence de transparence résultant en des modèles inintelligibles. C’est un problème qui se pose tout particulièrement en physique, domaine dans lequel on cherche à modéliser les lois régissant notre Univers sous la forme d’équations compréhensibles et non pas de réseaux de neurones opaques constitués de millions de nombres. Une équipe de recherche internationale comprenant des scientifiques du CNRS-INSU (voir encadré), s’est attaquée à ce problème en créant un algorithme d’intelligence artificielle produisant des modèles physiques analytiques à partir de données scientifiques brutes.
Manipuler des symboles mathématiques même élémentaires tels que l’addition ou la division peut s’avérer un défi complexe pour les réseaux de neurones. Toutefois, grâce aux progrès réalisés dans les techniques d'intelligence artificielle liées au traitement du langage et en s’appuyant sur les approches utilisées en calcul symbolique, il est désormais possible de créer des réseaux de neurones générant des équations. Néanmoins, la quête de l’équation idéale modélisant parfaitement un jeu de données en ayant la liberté conjuguer pléthore de symboles mathématiques peut rapidement devenir un enfer combinatoire. Comme on vous l’a peut être répété mainte fois à l’école, en physique on ne peut pas “additionner des patates et des carottes”, par exemple on ne peut pas additionner une longueur et une vitesse car cela n’a pas de sens physiquement. Ces règles dites d’analyse dimensionnelle interdisent certaines combinaisons de symboles mathématiques lors de l’écriture d’une équation physique et permettent de grandement réduire l'espace combinatoire.
La méthode d’intelligence artificielle baptisée “PhySO” acronyme d’Optimisation Symbolique Physique élabore des milliers d’équations par seconde et apprend de façon autonome à formuler des équations de qualité croissante par essai erreur tout en capitalisant sur ces règles d’analyse dimensionnelle. Il convient de souligner l'absence de préjugés de ce type de méthode non supervisée quant à la configuration précise des équations recherchées. Ce type d’impartialité intrinsèque pourrait-il un jour conduire à une recherche scientifique plus agnostique ?
Laboratoires impliqués
Laboratoire CNRS :
- Observatoire astronomique de Strasbourg (ObAS)
Tutelles : CNRS / Univ. Strasbourg
Autre laboratoire :
- Agence scientifique nationale australienne, CSIRO
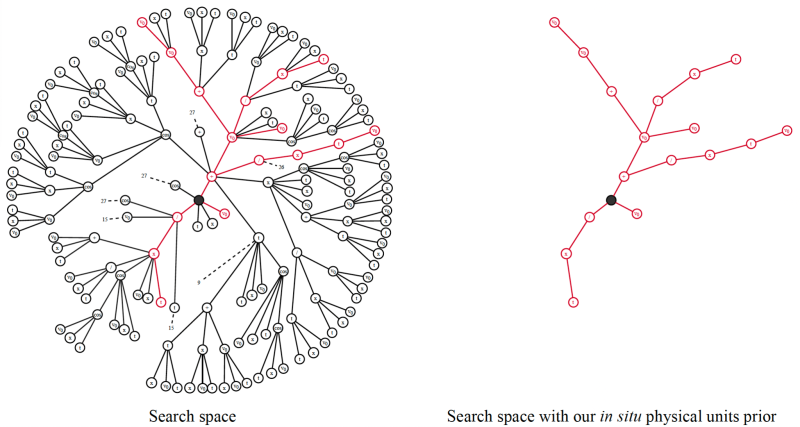
PhySO l’intelligence artificielle développée par la collaboration franco-australienne retrouvant l’équation du cas d’école de l'oscillateur harmonique à partir d’un jeu de données.
Audiodescription
Pour en savoir plus
Wassim Tenachi, Rodrigo Ibata, Foivos Diakogiannis, Deep symbolic regression for physics guided by units constraints: toward the automated discovery of physical laws, The Astrophysical Journal, 2023.
